¿Qué partícula subatómica se descubrió con este experimento?
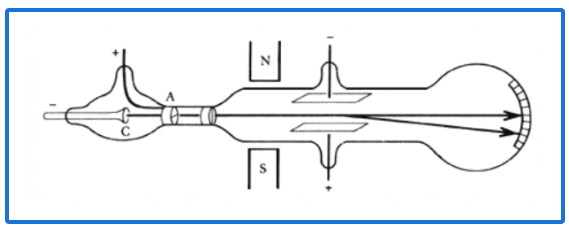
Electrones
¿Qué muestra el siguiente diagrama y para qué se utiliza?

El orden de llenado de los electrones en los orbitales en orden creciente de energía.Se usa para hacer las configuraciones electrónicas de los átomos.
¿Cuál es el nombre de los elementos representados por los símbolos que se indican?
Mg
Br
Mn
B
Mg: Magnesio
Br: Bromo
Mn: Manganeso
B: Boro
¿Cuál es la capa de valencia de los elementos del grupo 1 y qué carga tiene el ion más estable que forman?
ns1
Carga +1
¿Cuántos protones,neutrones y electrones tiene un átomo neutro con Z=11 y A=23?
11 protones
11 electrones
12 neutrones
¿Qué tres tipos de enlace químico se pueden dar entre los átomos?
Enlace iónico
Enlace covalente
Enlace metálico
¿Cuáles de las siguientes moléculas son polares?Justifica tu respuesta.
a) I2
b) HI
c) H2O
Son polares el yoduro de hidrógeno y el agua, pues el enlace covalente se da entre átomos distintos.
¿Qué modelo atómico representa esta imagen?
Explica cómo es el átomo según dicho modelo.
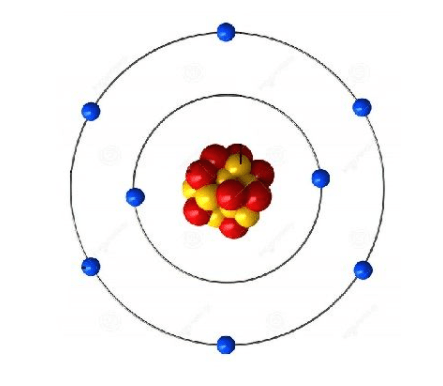
Modelo atómico de Böhr
El átomo está formado por un núcleo donde se encuentran protones y neutrones,y una corteza donde se encuentran los electrones moviéndose en determinadas órbitas,en determinadas capas o niveles donde tienen cierta energía.
¿Cuántos electrones puede haber como mucho en cada orbital?
2 electrones con espines contrarios.
¿Cuántos grupos y periodos hay en la tabla periódica?
18 grupos y 7 periódos
¿En qué grupo y período se encuentra el helio?
Grupo 18,período 1
¿Cuál es la carga de un átomo que tiene 16 neutrones,16 protones y 18 electrones?
¿Es un catión,anión o átomo neutro?
Es un anión con carga -2
¿Cuál es el enlace químico que tiene lugar en la sal común (NaCl)? Justifica tu respuesta.
Se da enlace iónico, puesto que tiene lugar entre átomos de un metal (Na) y átomos de un no metal (Cl).
¿Qué fuerzas intermoleculares se dan entre las moléculas de cloro?
Fuerzas de Van der Waals (London).
¿Qué modelo atómico representa esta imagen?
Explica cómo es el átomo según dicho modelo.
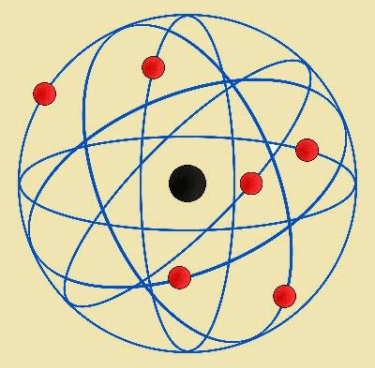
Modelo atómico de Rutherford.
El átomo está formado por un núcleo pequeño donde está la carga positiva(protones) y se concentra casi toda la masa del átomo,espacio vacío y los electrones giran alrededor del núcleo en la corteza, describiendo órbitas planetarias.
Escribe la configuración electrónica del potasio(Z=19).
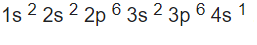
¿Qué tienen en común los elementos de un mismo grupo?
Los mismos electrones en la capa de valencia y, por ello,comportamiento químico similar.
Ordena en orden creciente de tamaño los siguientes átomos:
I,F,Br,Cl
F<Cl<Br<I
Todos los átomos de un mismo elemento tienen el mismo número de:
a)electrones
b)protones
c)neutrones
protones
En este tipo de enlace, los átomos comparten electrones para completar el octeto.
Enlace covalente.
¿Qué fuerzas intermoleculares se dan entre las moléculas de amoniaco?
Enlaces de hidrógeno (puentes de hidrógeno).
Indica a qué modelo hace referencia la siguiente frase:
El átomo es una "bola" cargada positivamente en la que están incrustados los electrones.
Modelo atómico de Thomson
El oxígeno tiene como número atómico z= 8.¿Cuál de las siguientes distribuciones electrónicas en sus orbitales,indicados mediante cajas, es la correcta y por qué?
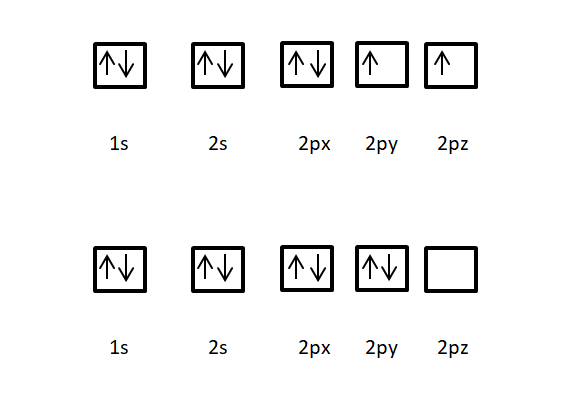
La correcta es la primera porque primero se llenan los electrones con espines paralelos y luego se van llenando con espines contrarios,por ser así el átomo más estable.
¿Cuál es la capa de valencia de los gases nobles y qué particularidad presentan respecto a su comportamiento químico debido a esos electrones de valencia?
ns2np6
8 electrones en la capa de valencia(regla del octeto),octeto completo. Son estables y no se unen con otros átomos.
Ordena en orden creciente de tamaño los siguientes átomos:
S,Al,Na,Si
S<Si<Al<Na
Los isótopos son átomos de un mismo elemento con distinto número:
a) másico
b)atómico
Distinto número másico,distinto número de neutrones.
¿Qué enlace se da entre los átomos de oro?
Explica cómo se forma dicho enlace.
Enlace metálico
Nube electrónica
¿Cuál de las siguientes sustanciasa no conduce la electricidad en estado sólido, pero sí la conduce fundida o disuelta? Justifica tu respuesta.
a) CaF2
b) Cu
c) H2O
a) CaF2, por ser un compuesto iónico.
¿En qué modelo atómico apareció el concepto de orbital?
Modelo atómico actual
¿Cuáles son los electrones de valencia de los siguientes átomos?

A: 1s2
B: 3s1
C: 3s23p5
D:3d5
¿Cuál será el ion más estable que formará el fluor (z=9)?
F-: 1s22s22p6
Clasifica los siguientes elementos en metales y no metales:
Oxígeno Cloro
Litio Platino
Zinc Manganeso
Metales: Li,Pt,Zn,Mn
No metales: O,Cl
Las partículas subatómicas con masa despreciable son los .......... y tienen carga ...........
electrones
negativa
Representa el diagrama de Lewis de la molécula de agua.
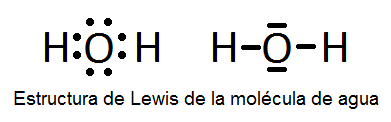
Enumera tres propiedades del diamante, explicando para ello el tipo de enlace que se da entre sus átomos y la estructura que se forma.
Átomos de carbono unidos mediante enlace covalente formando un cristal.
-Muy duro.
-Elevadas temperaturas de fusión y ebullición.
-No conduce la electricidad.